種類の異なる原子において、一方の原子が持つ電子が、他方の原子に完全に移ることによって、原子同士が互いに引き合うことでできる結合。
電気陰性度が大きく異なる原子同士は、電子を共有するよりも、電子を一方の原子に移したり受け取ったりするほうが最外殻を満たしやすいため、イオン結合が起こる。
なお、イオン結合だけで結びついているイオンは、一般的に「塩」と呼ばれる。分子は共有結合をつくるものを指す。
イオン結合がおこる過程(NaClを例に)
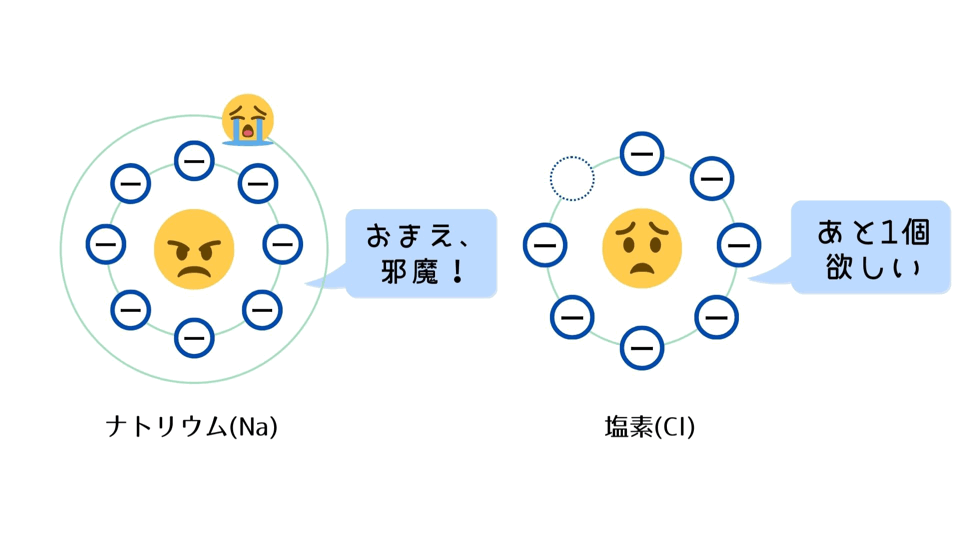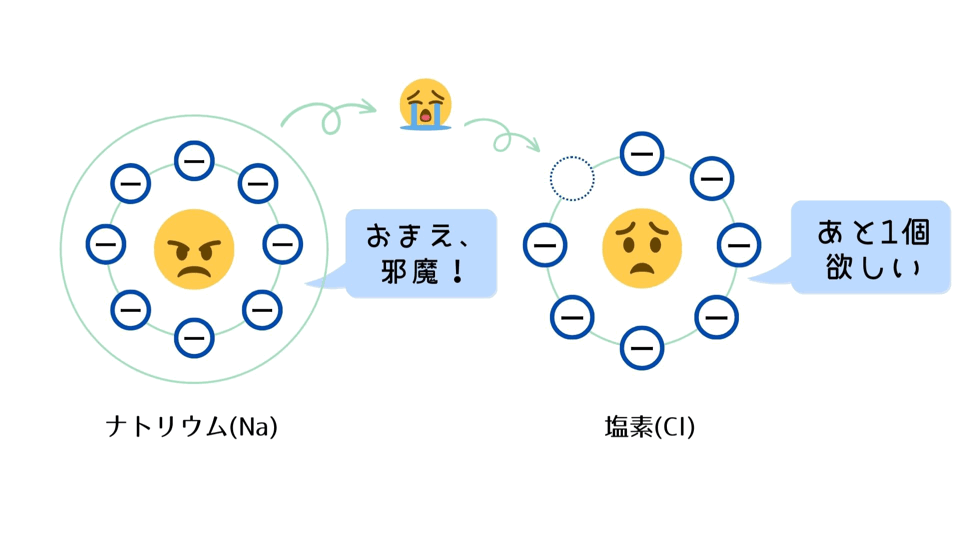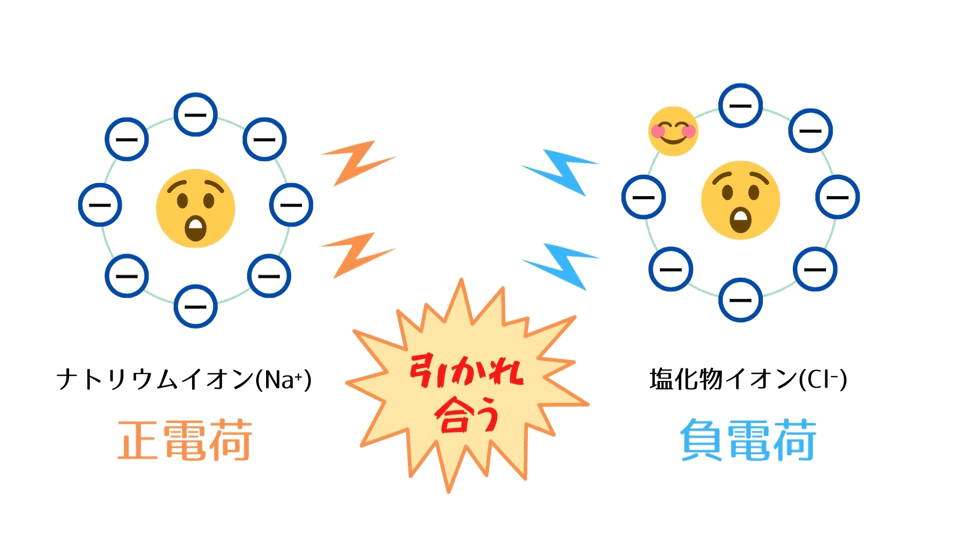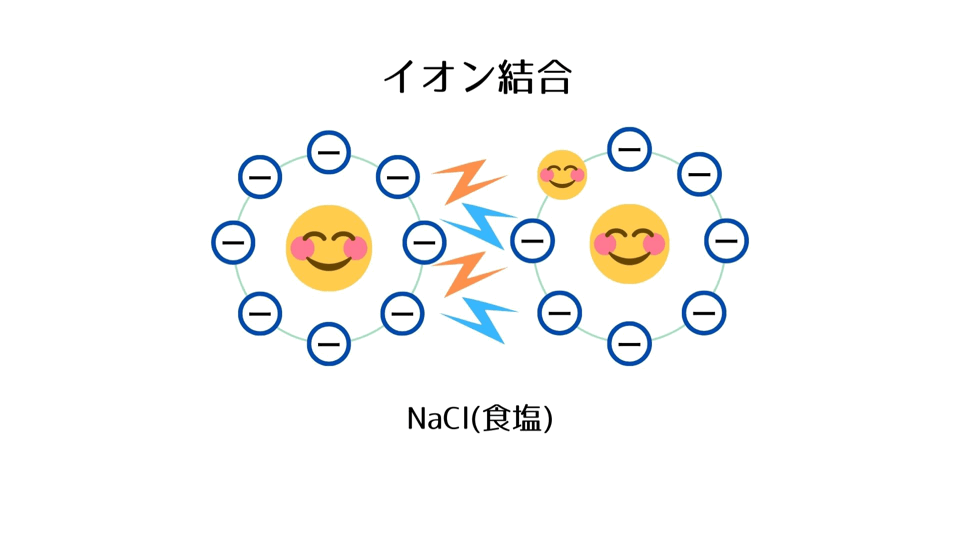
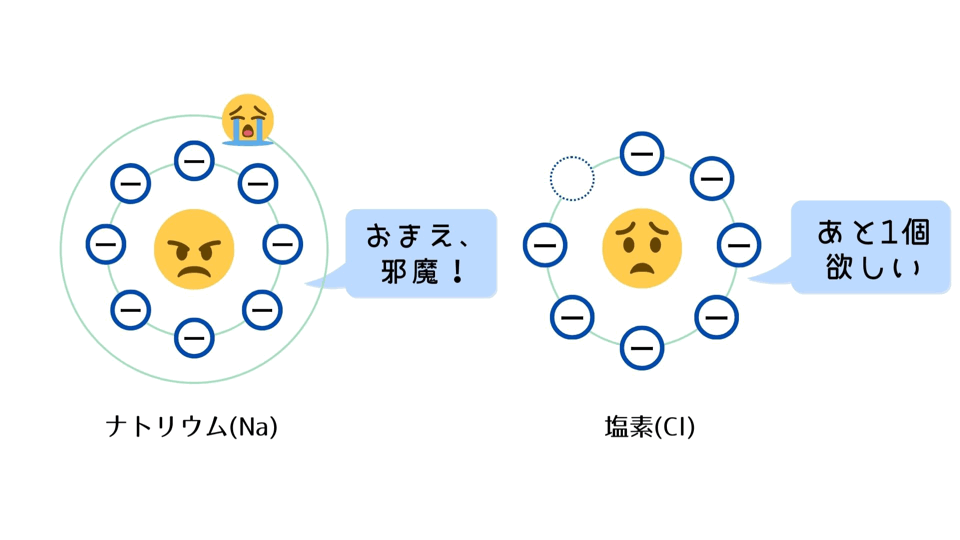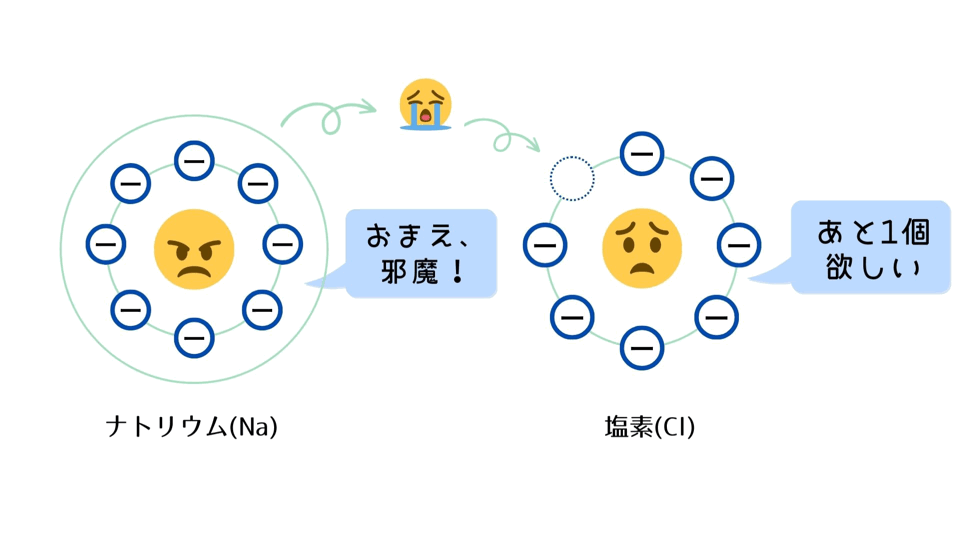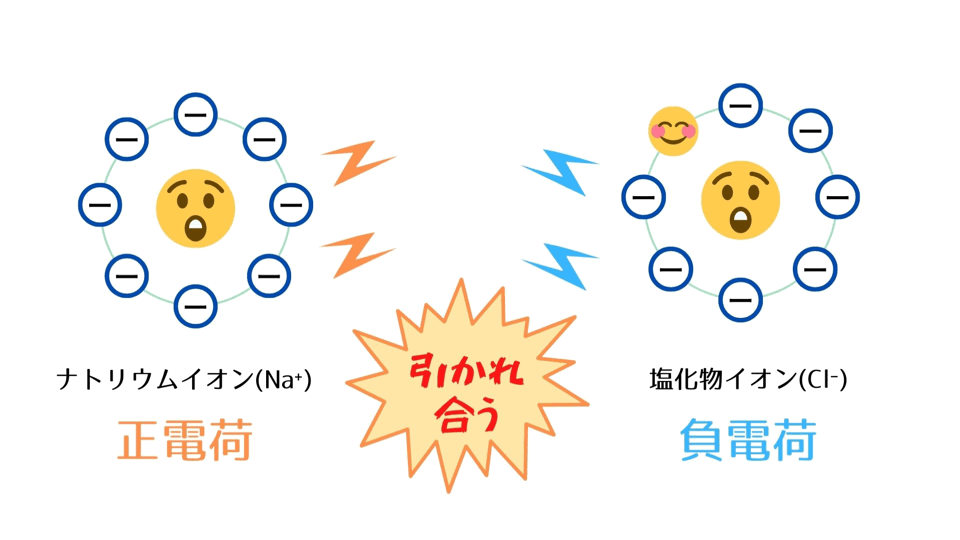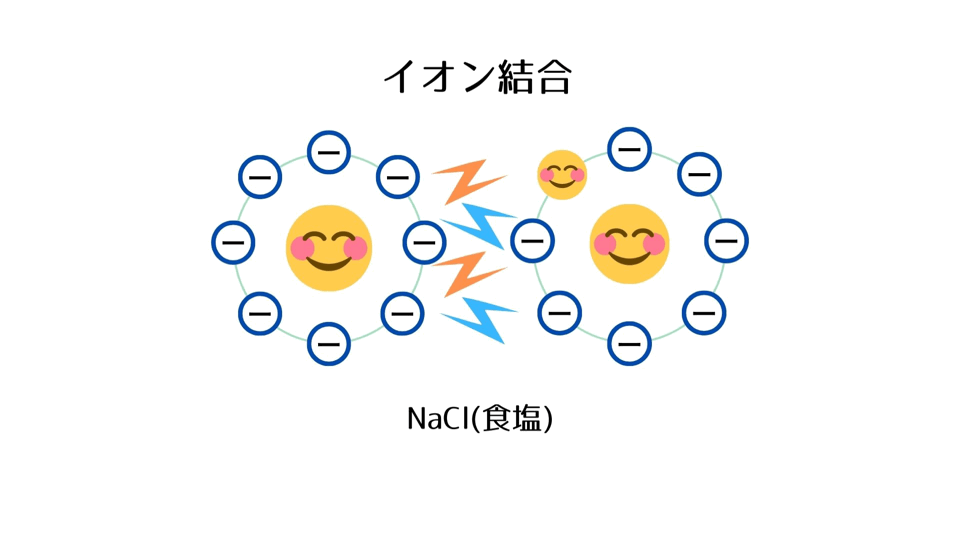
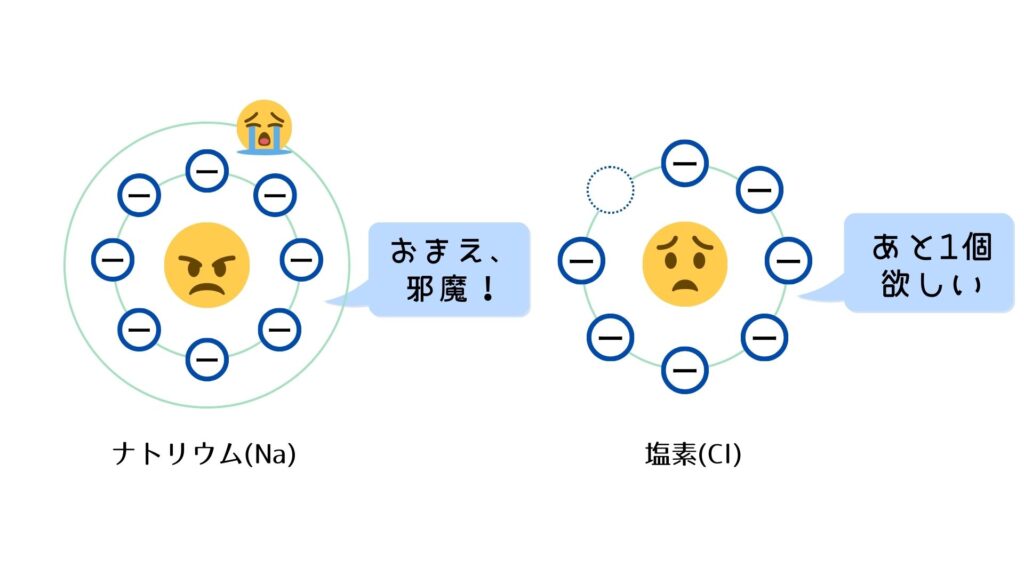
① 原子は、最外殻の電子を満たしたい。
・ナトリウム(Na)は、最外殻に電子がひとつあるだけなので、電子を放出すれば最外殻が満たされる。
・塩素(Cl)は、最外殻に電子がもうひとつあれば、最外殻が満たされる。
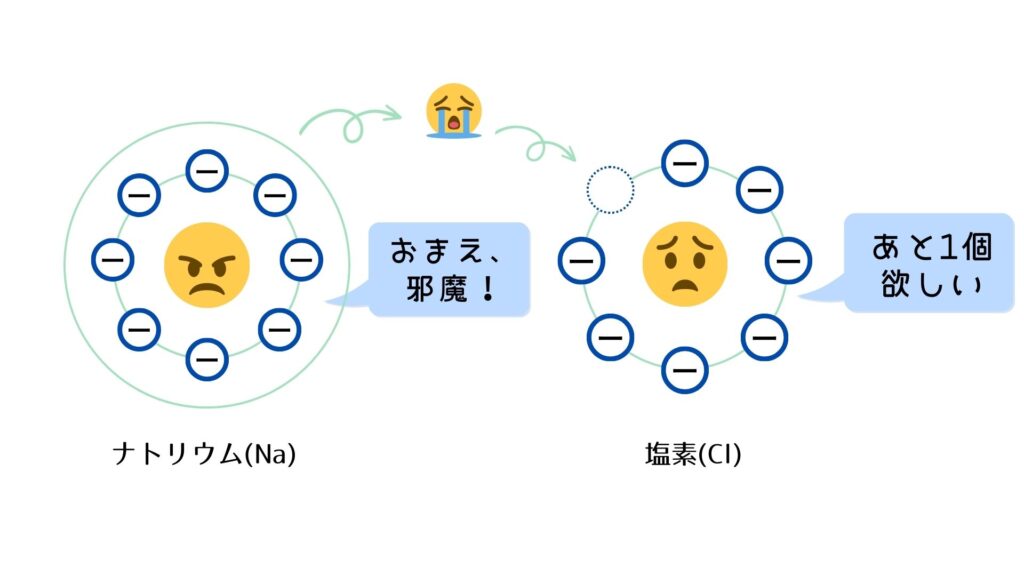
② NaとClが出会うと、Naの電子が飛び出し、Clに移動し、それぞれの原子がイオンになる。
・電子を1個失ったNaは1価の正電荷を持つことになり、ナトリウムイオン(Na⁺)になる。
・電子を1個受け取ったClは1価の負電荷を持つことになり、塩化物イオン(Cl⁻)になる。
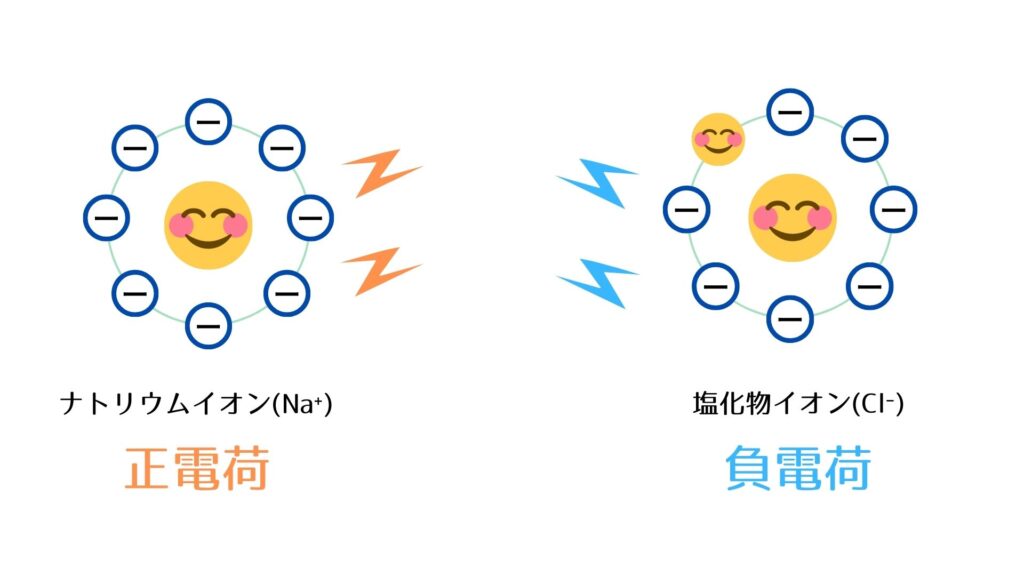
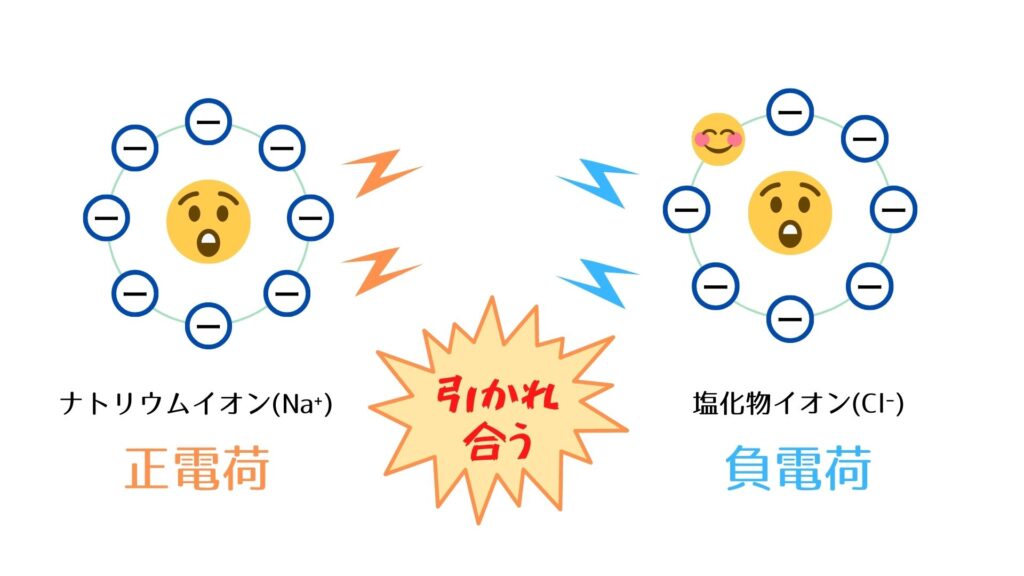
③ 反対の電荷を持つNa⁺とCl⁻は互いに引き合い、イオン結合をつくり、NaCl(食塩)となる。

- 古細菌
- C値パラドックス
- DNAポリメラーゼ
- 刺激
- 水素結合
- hydrogen bond
- 親水性
- hydrophilic
- 疎水性
- hydrophobic
- interphase
- mitotic phase
- M期
- 分裂期
- RNA干渉
- セイバー・ベビー
- 救世主ベビー
- savior sibling
- savior baby
- アーキア
- アクアポリン
- アクチビン
- アクチンフィラメント
- アセチルCoA
- アデニル酸シクラーゼ
- アボガドロ定数
- アミノ酸
- アロステリック酵素
- アンチコドン
- イオン結合
- ionic bond
- インテグリン
- エキソヌクレアーゼ
- エストロゲン
- オートクリン
- クリステ
- グロブリン
- クロマチン
- ゲノム
- コドン
- ゴルジ体
- シアノバクテリア
- シストロン
- センチモルガン
- チャネル
- チラコイド
- ドメイン
- トランスポゾン
- トリソミー
- ヌクレオチド
- ノックアウト
- バクテリオファージ
- ヘテロ二本鎖
- ヘミ接合
- ポリペプチド
- マイクロメートル
- ミトコンドリア
- メチレンブルー
- methylene blue
- モノソミー
- ヤヌスグリーンB
- Janus Green B
- リガンド
- リソソーム
- リボソーム
- 異化
- 遺伝子
- イデンシ
- 遺伝子型
- 遺伝子重複
- 一塩基多型
- 塩基
- 岡崎フラグメント
- 化合物
- 解糖系
- 核小体
- カクショウタイ
- 干渉
- 基質
- 極性
- polar
- 嫌気呼吸
- 嫌気性生物
- 検定交雑
- 原核生物
- 原形質
- 減数分裂
- 固定
- fixation
- 交叉
- 校正
- 酵素
- 細菌
- 細胞骨格
- サイボウコッカク
- 細胞質
- 細胞質基質
- サイボウシツキシツ
- 細胞小器官
- サイボウショウキカン
- 細胞説
- 自家不和合性
- 自然選択
- 受精
- ジュセイ
- 受動輸送
- ジュドウユソウ
- 受容器
- 受容細胞
- 受容体
- 収縮胞
- シュウシュクホウ
- 縮合反応
- 小胞体
- 常染色体
- 浸透度
- 真核生物
- シンカクセイブツ
- 酢酸オルセイン液
- aceto-orcein
- 酢酸カーミン液
- acetocarmine
- 水素結合
- 生活環
- 生体膜
- セイタイマク
- 染色体
- 染色体地図
- 挿入配列
- 相同染色体
- ソウドウセンショクタイ
- 他面発現
- 多型
- 体細胞
- タイサイボウ
- 体細胞分裂
- タイサイボウブンレツ
- 対合
- タイゴウ
- 対立遺伝子
- 代謝
- 単相
- タンソウ
- 中心体
- チュウシンタイ
- 電気陰性度
- electronegativity
- 動原体
- ドウゲンタイ
- 同化
- 内分泌
- 二価染色体
- ニカセンショクタイ
- 二倍体
- ニバイタイ
- 粘菌
- 能動輸送
- ノウドウユソウ
- 配偶子
- ハイグウシ
- 配偶体
- 伴性遺伝
- 表現型
- 表現度
- 表現模写
- 複相
- 併発率
- 変更遺伝子
- 胞子体
- 傍分泌
- 連鎖
- 胚